
Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
for tidlig graviditet
Medisinsk ekspert av artikkelen
Sist anmeldt: 04.07.2025
Posttermingraviditet er et av problemene som tradisjonelt sett avgjør stor vitenskapelig og praktisk interesse, først og fremst forårsaket av ugunstige perinatale utfall i denne patologien.
I innenlandsk obstetrikk antas det at et svangerskap etter termin, som varer i mer enn 287–290 dager, er ledsaget av intrauterin lidelse hos fosteret og ender med fødselen av et barn med tegn på biologisk overmodenhet, noe som bestemmer den høye risikoen for å utvikle ante/intranatalt distresssyndrom og vanskelig nyfødttilpasning.
Epidemiologi
Forekomsten av graviditet etter termin er omtrent 7 % av alle graviditeter (Martin et al., 2007).
Det amerikanske kollegiet for obstetrikere og gynekologer definerer posttermingraviditet som en som varer i mer enn 42 uker (294 dager). Forekomsten er i gjennomsnitt omtrent 10 %. I de fleste europeiske land defineres posttermingraviditet som en som varer i 294 dager eller mer, med unntak av Portugal (287 dager eller mer) og Irland (292 dager eller mer). Forekomsten av posttermingraviditet i Europa er omtrent 3,5–5,92 %.
Samtidig er ikke et barn med tegn på postmodenhet alltid født postmodent, og tvert imot kan tegn på postmodenhet observeres hos et foster født før utløpet av 290 dager i svangerskapet, noe som sannsynligvis skyldes individuell timing og trekk ved svangerskapsutviklingen. Imidlertid fortjener den funksjonelle tilstanden til et postmodent foster mer oppmerksomhet, gitt den høye hyppigheten av forekomst av slike alvorlige komplikasjoner som mekoniumaspirasjonssyndrom, hypoksisk-iskemisk skade på sentralnervesystemet, myokard, nyrer, tarmer, som fører til fosterdød før og under fødsel.
Posttermingraviditet regnes som en faktor som øker hyppigheten av komplikasjoner under fødsel og fører til en økning i perinatal sykelighet og dødelighet. De vanligste perinatale komplikasjonene ved posttermingraviditet er dødfødsel, asfyksi og fødselstraumer. E. Ya. Karaganova, IA Oreshkova (2003), etter å ha utført en grundig analyse av perinatale utfall hos 499 pasienter med posttermingraviditet avhengig av svangerskapsalder, fant at når svangerskapsalderen øker fra 41 til 43 uker, øker andelen perinatal sykelighet. Ved 43 ukers svangerskap øker dermed hyppigheten av hypoksisk-iskemisk CNS-skade med 2,9 ganger, asfyksi - med 1,5 ganger, aspirasjonssyndrom - med 2,3 ganger sammenlignet med fullbårne nyfødte med en svangerskapsalder på ikke mer enn 41 uker. Ved en graviditetsperiode på mer enn 41 uker ble tegn på fosterskade før fødselsstart oppdaget hos 67,1 % av fostrene (hos halvparten av dem ved en graviditetsperiode på 42–43 uker), blanding av mekonium i fostervannet - hos 31,6 %, oligohydramnion - hos 50,9 % av pasientene.
Fører til for tidlig graviditet
Den vanligste årsaken til graviditet etter termin er unøyaktig datering (Neilson, 2000; Crowley, 2004). Bruk av standard kliniske kriterier for å bestemme estimert fødselsdato (EDD) har en tendens til å overestimere svangerskapsalderen og øker derfor forekomsten av graviditet etter termin (Gardosi et al., 1997; Taipale og Hiilermaa, 2001). Kliniske kriterier som vanligvis brukes for å bekrefte svangerskapsalder inkluderer siste menstruasjon (LMP), livmorstørrelse vurdert ved bimanuell undersøkelse i første trimester, oppfatning av fosterbevegelser, auskultasjon av fosterets hjertelyder og fundushøyde. Enkeltbarnsgraviditet.
Når et svangerskap etter termin oppstår, er årsaken vanligvis ukjent.
Risikofaktorer
Ved analyse av den somatiske, obstetriske og gynekologiske anamnesen, og egenskapene til det nåværende svangerskapet, bemerkes risikofaktorer som indikerer muligheten for å utvikle et posttermin- og langvarig svangerskap.
Risikofaktorer for graviditet etter termin:
- den gravide kvinnen er over 30 år gammel;
- historie med seksuelt overførbare infeksjoner (SOI) og kroniske inflammatoriske sykdommer i livmorvedhengene;
- indikasjon på en historie med forsinket levering;
- "umoden" eller "utilstrekkelig moden" livmorhals ved 40 ukers svangerskap eller mer.
Risikofaktorer for langvarig graviditet:
- den gravide kvinnens alder er fra 20 til 30 år;
- dysfunksjon i eggstokkene med uregelmessig eller langvarig (≥ 35 dager) menstruasjonssyklus;
- avvik mellom svangerskapsalderen bestemt ut fra den første dagen i siste menstruasjon og ultralydsskanning.
Generelle risikofaktorer inkluderer førstegangsfødende kvinne, tidligere graviditet etter termin (Alfirevic og Walkinshaw, 1994; Mogren et al., 1999; Olesen et al., 1999), guttefoster (Divon et al., 2002), fedme (Usha Kiran et al., 2005; Stotland et al., 2007), hormonelle faktorer og genetisk predisposisjon (Laursen et al., 2004).
Det er ikke kjent hvordan kroppsmasseindeks (BMI) påvirker svangerskapsvarighet og fødselstidspunkt, men interessant nok har overvektige kvinner større sannsynlighet for å oppleve graviditet etter termin (Usha Kiran et al., 2005), mens kvinner med lav BMI har høyere risiko for graviditet etter termin og for tidlig fødsel (fødsel før 37 ukers svangerskap) (Hickey et al., 1997). Siden fettvev er hormonelt aktivt (Baranova et al., 2006) og overvektige kvinner kan ha endret metabolsk status, er det mulig at endokrine faktorer involvert i fødselsstart er endrede hos overvektige kvinner.
Genetiske faktorer kan være assosiert med forlenget svangerskap. Kvinner som selv har hatt et svangerskap etter termin, har høyere risiko for å få et svangerskap etter termin (relativ risiko på 1,3) (Mogren et al., 1999). Kvinner som har hatt et tidligere svangerskap etter termin, har økt risiko for å få et påfølgende svangerskap etter termin (27 % med ett tidligere svangerskap etter termin og 39 % med to tidligere langvarige svangerskap) (Kistka et al., 2007).
Patogenesen
Patogenesen til posttermingraviditet er ikke fullt ut forstått. Som vist ovenfor har noen risikofaktorer forbundet med posttermingraviditet blitt identifisert med noen mulige forklaringer. Patogenesen til denne tilstanden er imidlertid ennå ikke klar. Til tross for forbedringen i forståelsen av fødsel de siste årene, mangler vi fortsatt klarhet om de nøyaktige mekanismene som starter fødsel og fremmer dens progresjon. For å bedre forstå patogenesen til posttermingraviditet er det viktig å belyse patofysiologien til fødsel og prøve å forstå hvorfor disse mekanismene ikke utløses i posttermingraviditet, eller omvendt, utløses tidligere ved for tidlig fødsel. Det virker logisk at det faktisk er et felles grunnlag eller en felles sammenheng mellom disse tre tilstandene. Mekanismene ved fødsel involverer samspillet mellom hormonelle, mekaniske og inflammatoriske prosesser der morkaken, mor og foster spiller en viktig rolle.
Placental produksjon av kortikotropinfrigjørende peptid (CRH) er assosiert med svangerskapets varighet (McLean et al., 1995). Placental CRH-syntese øker eksponentielt etter hvert som svangerskapet utvikler seg og topper seg ved fødselen. Kvinner som føder for tidlig har en raskere eksponentiell vekstrate enn kvinner som føder til termin, mens kvinner som føder senere har en lavere vekstrate (Ellis et al., 2002; Torricelli et al., 2006). Disse dataene antyder at postterminfødsel skyldes endrede biologiske mekanismer som regulerer svangerskapets varighet. Dette kan skyldes en arvelig predisposisjon som følge av polymorfismer i gener i den fysiologiske banen som knytter CRH til fødsel. Det er også mulig at mors fenotype kan endre responsen til morsvevet på normale hormonelle signaler ved fødselen, slik det kan forekomme hos overvektige kvinner.
CRH kan direkte stimulere fosterets binyrer til å produsere DHEA, en forløper for syntese av østriol i placenta (Smith et al., 1998). CRH-konsentrasjoner i mors plasma korrelerer med østriolkonsentrasjoner (Smith et al., 2009). Den CRH-induserte økningen i østriol øker raskere enn østradiolnivåene sent i svangerskapet, noe som resulterer i et økt forhold mellom østriol og østradiol som antas å skape et østrogent miljø i de siste ukene av svangerskapet. Samtidig avtar eller til og med avtar økningen i mors plasmaprogesteron som oppstår under graviditeten, sent i svangerskapet. Dette kan skyldes CRH-hemming av progesteronsyntese i placenta (Yang et al., 2006). Dermed avtar den graviditetsfremmende (avslapningsfremmende) effekten av progesteron etter hvert som den fødselsfremmende (livmorkontraksjonsfremmende) effekten av østriol øker. Disse endringene i forholdstall har blitt observert i premature, terminfødte enlingssvangerskap og tvillingsvangerskap (Smith et al., 2009). Situasjonen ved svangerskap etter termin er ukjent.
Symptomer for tidlig graviditet
Symptomkomplekset ved et overmodent foster ble først beskrevet av Ballantyne (1902) og Runge (1948), og det er derfor det kalles Ballantyne-Runge syndrom, inkludert fravær av osteaktig fett, tørrhet og maserasjon av huden til den nyfødte ("bade"-føtter, håndflater), samt i lyske- og aksillære folder, lange negler, tette bein i hodeskallen, smale suturer og reduserte fontaneller, grønnaktig eller gulaktig farging av huden, fosterhinner og navlestreng. Andre observasjoner indikerer langvarig graviditet.
Langvarig graviditet, som varer i mer enn 287 dager, er ikke ledsaget av fosterlidelser og ender med fødselen av et friskt barn uten tegn på overmodenhet. Dermed regnes langvarig graviditet som en fysiologisk tilstand som tar sikte på fosterets endelige modning.
Komplikasjoner og konsekvenser
Posttermingraviditet er assosiert med økt mobilitet og sykelighet hos fosteret og nyfødte, samt mors sykelighet. Disse risikoene er større enn opprinnelig antatt. Tidligere ble risikoene undervurdert av to grunner. For det første ble tidligere studier av posttermingraviditet publisert før ultralyd ble en rutinemessig metode for å definere graviditet. Som et resultat var mange av svangerskapene som ble inkludert i studiene, faktisk ikke posttermin. Den andre grunnen er knyttet til selve definisjonen av dødfødsel. Dødfødselsrater har tradisjonelt blitt beregnet ved hjelp av svangerskap født ved en gitt svangerskapsalder, snarere enn pågående (ufødte) svangerskap. Dette vil redusere dødfødselsraten i posttermingraviditeter, siden når fosteret er født, ikke lenger er i fare for intrauterin fosterdød (IUFD). Dermed er den passende nevneren ikke alle fødsler ved en gitt svangerskapsalder, men pågående (ufødte) svangerskap (Rand et al., 2000; Smith, 2001; Caughey et al., 2003).
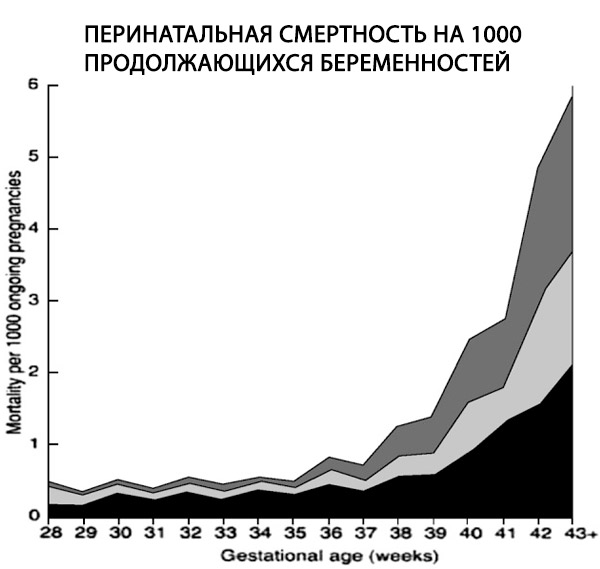
En retrospektiv studie av over 170 000 enlingsfødsler ved bruk av en passende nevner viste en seksdobling i dødfødselsraten i postterminsvangerskap fra 0,35 til 2,12 per 1000 pågående svangerskap (Hilder et al., 1998).
Komplikasjoner hos fosteret og nyfødt
Perinatal dødelighet, definert som dødfødsler pluss tidlige nyfødtdødsfall, er dobbelt så høy ved 42 ukers svangerskap som ved termin (henholdsvis 4–7 versus 2–3 per 1000 fødsler). Den øker fire ganger ved 43 uker og fem til syv ganger ved 44 uker (Bakketeig og Bergsjo, 1989; Feldman, 1992; Hilder et al., 1998; Cotzias et al., 1999). Disse dataene viser også at når det beregnes per 1000 pågående svangerskap, øker foster- og nyfødtdødeligheten kraftig etter 40 uker (Hilder et al., 1998) (Hilder et al., 1998).
Uteroplacental insuffisiens, mekoniumaspirasjon og intrauterin infeksjon anses å være hovedårsakene til den økte perinatale dødeligheten i disse tilfellene (Hannah, 1993).
Fostermorbiditet er også økt i svangerskap etter termin og svangerskap som går utover 41 ukers svangerskap. Dette inkluderer mekoniumpassasje, mekoniumaspirasjonssyndrom, makrosomi og dysmaturitet. Svangerskap etter termin er også en uavhengig risikofaktor for lav pH i navlestrengen (neonatal acidemi), lav 5-minutters Apgar-skåre (Kitlinski et al., 2003), neonatal encefalopati (Badawi et al., 1998) og spedbarnsdødelighet i løpet av det første leveåret (Hilder et al., 1998; Cotzias et al., 1999; Rand et al., 2000). Selv om noen av disse spedbarnsdødsfallene tydelig er et resultat av perinatale komplikasjoner som mekoniumaspirasjonssyndrom, har de fleste en ukjent årsak.
Omtrent 20 % av postmature fostre har dysmaturitetssyndrom, som refererer til nyfødte med trekk som ligner kronisk intrauterin veksthemming på grunn av uteroplacental insuffisiens (Vorherr, 1975; Mannino, 1988). Disse inkluderer tynn, rynkete, flassende hud (overdreven flassing), tynn kropp (underernæring), langt hår og negler, oligohydramnion og hyppig passasje av mekonium. Disse gravide kvinnene har økt risiko for navlestrengskompresjon på grunn av oligohydramnion, mekoniumaspirasjon og kortsiktige neonatale komplikasjoner som hypoglykemi, anfall og respirasjonssvikt.
Risikoer for mor
Posttermin graviditet er forbundet med betydelig risiko for moren. Risikoen er økt:
- fødselsdystoki (9–12 % mot 2–7 % ved full termin);
- alvorlige perineale sår (3. og 4. grads sår) assosiert med makrosomi (3,3 % mot 2,6 % ved full termin);
- operativ vaginal fødsel; og
- dobling av keisersnittraten (14 % mot 7 % ved termin) (Rand et al., 2000; Campbell et al., 1997; Alexander et al., 2000; Treger et al., 2002).
Keisersnitt er assosiert med en høyere forekomst av endometritt, blødning og tromboembolisk sykdom (Alexander et al., 2001; Eden et al., 1987).
I likhet med nyfødte utfall øker morsmorbiditeten også med termingraviditet opptil 42 ukers svangerskap. Komplikasjoner som korioamnionitt, alvorlige perineale sår, keisersnitt, postpartum blødning og endomyometritt øker etter 39 ukers svangerskap (Yoder et al., 2002; Caughey og Bishop, 2006; Heimstad et al., 2006; Caughey et al., 2007; Bruckner et al., 2008;).
Diagnostikk for tidlig graviditet
Tradisjonell diagnostikk av posttermin graviditet består av tilstrekkelig beregning av svangerskapsalderen. Samtidig inkluderer de mest nøyaktige metodene på nåværende tidspunkt beregninger basert på den første dagen i siste menstruasjon og ultralyddata fra 7. til 20. svangerskapsuke. En rekke forfattere anser disse to metodene som likeverdige. Noen forskere foreslår imidlertid å utelukkende stole på ultralydbiometridata når man bestemmer svangerskapsalderen i posttermin graviditet. Blant risikofaktorene for posttermin graviditet skilles en rekke trekk ved den somatiske, obstetriske og gynekologiske anamnesen og forløpet av det nåværende svangerskapet.
Fra den somatiske anamnesen fremhever mange forfattere foreldrenes alder over 30 år, tilstedeværelsen av ekstragenital patologi hos moren. Blant trekkene ved den obstetriske og gynekologiske anamnesen bør man være oppmerksom på menstruasjonsdysfunksjon, tilstedeværelsen av aborter og spontanaborter, inflammatoriske sykdommer i livmorvedhengene, en historie med forsinket fødsel og 3 eller flere kommende fødsler.
Laboratoriediagnostikk av posttermin graviditet
Etter hvert som graviditetsperioden etter termin øker, skjer en progressiv reduksjon av kallekrein-kinin-systemet, noe som manifesterer seg i ekstremt lavt kininogeninnhold (0,25–0,2 μg/ml, med N=0,5 μg/ml), lav aktivitet av kallekrein, dets hemmere og spontan esteraseaktivitet i blodplasma etter 41 ukers svangerskap.
I posttermin graviditet observeres intensivering av lipidperoksidasjonsprosesser både i den gravide kvinnens kropp og i fosterets kropp, noe som bidrar til hemming av membranbindende enzymer i subcellulære strukturer. Som et resultat svekkes avgiftnings- og energiproduksjonsfunksjonene betydelig, og som en konsekvens akkumuleres eksogene og endogene toksiske metabolitter, og endotoksemi utvikles, som forverres etter hvert som svangerskapet øker. Intensiteten av endotoksemi kan vurderes ved hjelp av erytrocytters sorpsjonskapasitet og konsentrasjonen av mellomstore molekylære proteiner. En økning i peroksidasjon og endogen forgiftning korrelerer med alvorlighetsgraden av føtal hypoksi.
Posttermingraviditet er preget av et lavt innhold av prostaglandin F2α, som syntetiseres i decidua og myometrium og er den viktigste modulatoren for utviklingen av fødsel.
Ved en graviditetsperiode på mer enn 41 uker observeres en økning i plasmaviskositet, urinsyrekonsentrasjon og en reduksjon i konsentrasjonen av fibrinogen, antitrombin III og blodplatetall. Konsentrasjonen av føtalt fibronektin > 5 ng/ml i cervikovaginal sekresjon hos kvinner med en graviditetsperiode på mer enn 41 uker indikerer en høy biologisk beredskap i kroppen for fødsel og spontan fødselsstart innen de neste 3 dagene. Sensitiviteten og spesifisiteten til denne metoden er henholdsvis 71 og 64 %.
Det er ekstremt viktig å studere funksjonstilstanden til det fetoplacentale komplekset og fosteret i posttermingraviditet (ultralyd, Doppler og kardiotokografiske studier). Under den ekkografiske studien utføres fetometri for å bestemme fosterets estimerte vekt og vurdere dets anatomiske utvikling. I 12,2 % av tilfellene oppdages IUGR av I–II grader, noe som ikke avviker signifikant fra hyppigheten av påvisning av syndromet ved langvarig graviditet. Samtidig oppdaget vi i 80 % av tilfellene en asymmetrisk form av IUGR og i 20 % - en symmetrisk form. Posttermingraviditet er preget av påvisning av ekkografiske tegn på uttalte involusjonsdystrofiske forandringer (GIII med petrifikasjoner). Gjennomsnittsverdien av fostervannsvolumindeksen i gruppen med posttermingraviditet var 7,25 ± 1,48, typisk for posttermingraviditet er påvisning av en redusert mengde fostervann.
Doppler-studie
Den viktigste faktoren for å forutsi perinatale utfall er å bestemme stadiene av fosterets hemodynamiske forstyrrelser under graviditet etter termin.
- Stadium I - forstyrrelse av intraplacental og føtoplacental blodstrøm. På dette stadiet er det ingen forstyrrelser i arteriell og venøs føtal hemodynamikk. En økning i vaskulær motstand observeres i navlestrengsarterien og dens terminale grener, så vel som i spiralarteriene. Indikatorene for gasssammensetning og syre-base-balanse i navlestrengsblodet er innenfor normale grenser.
- Stadium II - sentralisering av fosterets blodsirkulasjon. Hypoksemi observeres i blodet til den nyfødte ved fødselen. På dette stadiet skilles det mellom to påfølgende stadier.
- IIa - første tegn på sentralisering av føtal arteriell sirkulasjon med uendret venøs og intrakardial blodstrøm, karakterisert ved:
- en reduksjon i resistens i MCA (med ikke mer enn 50 %) eller en økning i vaskulær resistens i aorta;
- reduksjon av CPC (til 0,9);
- en økning i motstanden i fosterets nyrearterier med ikke mer enn 25% av normen.
- IIb - moderat uttrykt sentralisering av blodsirkulasjonen med nedsatt blodstrøm i venekanalen og økt blodstrøm på aortaklaffen. På dette stadiet oppdages følgende:
- samtidig økning i vaskulær motstand i aorta og reduksjon i den midtre hjernearterien;
- reduksjon i CPC;
- økning i gjennomsnittlig blodstrømningshastighet (Tamx) i venekanalen;
- økning i den gjennomsnittlige lineære og volumetriske blodstrømningshastigheten ved aortaklaffen.
- IIa - første tegn på sentralisering av føtal arteriell sirkulasjon med uendret venøs og intrakardial blodstrøm, karakterisert ved:
- Stadium III - uttalt sentralisering av fosterets sirkulasjon med nedsatt venøs utstrømning og dekompensasjon av sentral og intrakardial hemodynamikk. Hypoksemi kombinert med acidose og hyperkapni observeres i navlestrengsblodet til den nyfødte ved fødselen. Dopplerometriske indikatorer på dette stadiet er preget av:
- en reduksjon i vaskulær motstand i SMA med mer enn 50 % av normen, en reduksjon i CPC under 0,8;
- progressiv økning i vaskulær motstand i aorta og nyrearterier med mer enn 80 %;
- i venekanalen - en økning i S/A-forholdet, PIV (mer enn 0,78) og en reduksjon i Tamx;
- i vena cava inferior - en økning i PIV, IPI og %R (mer enn 36,8%);
- i halsvenene - en økning i S/A-forholdet, PIV (over 1,1) og en reduksjon i Tamx;
- en reduksjon i den gjennomsnittlige lineære og volumetriske hastigheten ved klaffene i aorta og lungestammen;
- økt hjertefrekvens, redusert slagvolum, venstre ventrikkels endesystoliske og endediastoliske volum og hjerteminuttvolum.
De identifiserte stadiene av fosterets hemodynamiske endringer gjenspeiler den jevne utviklingen av funksjonelle tilstandsforstyrrelser under tilstander med kronisk intrauterin hypoksi under posttermin graviditet. Når hypoksemi kombinert med hyperacidemi og hyperkapni oppdages i navlestrengsblodet til en nyfødt, er hyppigheten av negative perinatale utfall 4,8 ganger høyere sammenlignet med gruppen med isolert hypoksemi. Følgelig gjenspeiler hyperacidemi og hyperkapni uttalte fosterets metabolske forstyrrelser og progressiv forverring av fosterets tilstand under tilstander med kronisk hypoksi under posttermin graviditet.
Kardiotokografi
Når denne metoden utføres i stadium I, oppdages første tegn på kronisk intrauterin hypoksi (20,93 %) og moderat føtal hypoksi (6,97 %). I stadium IIa økte hyppigheten av første tegn på føtal hypoksi med 2 ganger, med moderat hypoksi - med 4,13 ganger. I stadium IIb øker hyppigheten av moderat og alvorlig føtal hypoksi betydelig. I stadium III ble kun alvorlig (65,1 %) og moderat (30,2 %) føtal hypoksi oppdaget.
Programmet for screeningundersøkelse av gravide inkluderer:
- identifisering av gravide kvinner med risiko for graviditet etter termin;
- ultralydfetometri med vurdering av tegn på modenhet hos det nyfødte;
- vurdering av mengden og kvaliteten på fostervann;
- vurdering av modenhetsgraden til morkaken;
- kardiotokografi;
- vurdering av føtal hemodynamikk (arteria cerebri media, aorta, venøs kanal, vena cava inferior);
- vurdering av fosterets biofysiske profil;
- vurdering av livmorhalsmodenhet;
- fostervannsskopi.
Hvordan undersøke?
Differensiell diagnose
Under en omfattende undersøkelse av kvinner med langvarig graviditet avsløres følgende:
- i 26,5 % av observasjonene - grad II, i 51,8 % - grad III placentamodning;
- i 72,3 % av observasjonene - normal mengde fostervann;
- i 89,2 % av observasjonene - normale indikatorer på føtal-placental blodstrøm og i 91,6 % - normalt cerebroplacentalt forhold;
- i 100% av observasjonene - normale indikatorer på fosterets sentrale hemodynamikk, dens transvalvulære og venøse blodstrøm;
- En reduksjon i CPC med normale indikatorer på føtal placenta og føtal blodstrøm indikerer tilstedeværelsen av avvik i fosterets funksjonelle tilstand og er karakteristisk for IUGR, intrauterin infeksjon og kronisk føtal hypoksi.
Hvem skal kontakte?
Behandling for tidlig graviditet
Nøyaktig datering av svangerskapet er avgjørende for diagnostisering og behandling av graviditet etter termin (Mandruzzato et al., 2010). Siste menstruasjon har tradisjonelt blitt brukt til å beregne forventet fødselsdato (EDD). Imidlertid kan det forekomme mange unøyaktigheter på grunn av uregelmessigheter i syklusen, nylig bruk av hormonell prevensjon eller blødning tidlig i svangerskapet.
Rutinemessig ultralydscreening for graviditet har vist seg å redusere andelen falskt positive diagnoser og dermed den totale andelen graviditeter etter termin fra 10–15 % til omtrent 2–5 %, og dermed minimere unødvendige inngrep (Bennett et al., 2004; Caughey et al., 2008a; 2009).
Målene med behandling av posttermin graviditet er: korrigering av fosterets hemodynamiske forstyrrelser, forebygging av fosterprogresjon under fødsel, forberedelse av fødselskanalen for fødsel, igangsetting av fødsel.
Indikasjoner for sykehusinnleggelse
Overskridelse av svangerskapsalderen på 40 uker og 3 dager med en nøyaktig beregnet fødselsdato, tilstedeværelse av risikofaktorer for graviditet etter termin og utilstrekkelig forberedt fødselskanal.
Medikamentell behandling av posttermin graviditet
For å korrigere fosterets tilstand under graviditet etter termin, brukes legemidlet hesobendin + etamivan + etofillin (instenon) - et kombinasjonsmedisin med en nevrobeskyttende effekt basert på gjensidig potensering av effekten av komponentene.
Indikasjoner for administrering av legemidlet hesobendin + etamivan + etofillin:
- nedsatt blodstrøm i fosterets navlestrengsarterie (SDO > 2,7, IR > 0,65);
- reduksjon i cerebroplacental koeffisient (CPC < 1,10);
- første tegn på sentralisering av fosterets sirkulasjon;
- Første tegn på fosterhypoksi i henhold til CTG-data. De listede faktorene som indikerer første tegn på fosterlidelser krever ikke akutt fødsel, men indikerer behovet for å korrigere tilstanden ved å øke fosterhjernens tilpasningsevne under fødselen.
Forberedelse til fødsel i posttermin graviditet
Mekaniske metoder for irritasjon i livmorhalsen:
- Løsning av den nedre polen på fosterblæren. Løsning av den nedre polen på fosterblæren kan også føre til økt syntese av prostaglandiner og "modning" av livmorhalsen. Løsning av den nedre polen på fosterblæren, utført daglig eller 2-3 ganger i uken, bidrar til å forberede livmorhalsen på fødsel og igangsette fødsel. Denne metoden er svært effektiv, enkel å utføre, har lav frekvens av bivirkninger og er billig. Ulempene inkluderer ubehag som den gravide kvinnen føler under undersøkelsen, sjeldne blødninger og muligheten for ruptur av fosterhinnene.
- Ballongutvidelse av livmorhalsen. For ballongutvidelse av livmorhalsen brukes et Foley-ballongkateter. Det settes inn og blåses opp i livmorhalskanalen. Denne metoden utvider livmorhalskanalen mekanisk og forbedrer syntesen av prostaglandiner. Gjennom kateteret er det mulig å introdusere en saltløsning i det ekstra-amniotiske rommet, noe som utvider det nedre livmorsegmentet og også letter fødselsstart.
- Mekaniske dilatatorer av naturlig og syntetisk opprinnelse. For å forberede livmorhalsen for fødsel brukes livmorhalsdilatatorer av naturlig opprinnelse - laminaria og syntetiske - dilapan, gipan, lamicel, som er sonder med en diameter på 2 til 4 mm og en lengde på 60-65 mm. Laminaria er laget av naturlig materiale fra algen Laminaria japonicum. Syntetiske dilatatorer er laget av kjemisk og biologisk inerte polymerer med god hygroskopisitet. Probene-dilatatorene settes inn i livmorhalskanalen i ønsket mengde. På grunn av sin hygroskopisitet absorberer de væsken som finnes i livmorhalskanalen, utvider seg betydelig og utøver radialt trykk på livmorhalskanalen. De åpner livmorhalsen mekanisk og letter fødselsstart. Syntetiske dilatatorer av livmorhalskanalen forårsaker ikke ubehag og tolereres godt av pasienter. Begrenset bruk av syntetiske dilatatorer er forbundet med forsiktighet på grunn av deres lange opphold i livmorhalskanalen, noe som øker risikoen for stigende infeksjon. De beskrevne mekaniske virkningsmetodene på livmorhalsen forårsaker en reaksjon på syntesen av endogene prostaglandiner E2 i livmorhalsen, noe som bidrar til en reduksjon i mengden og destabiliseringen av kollagen i strukturen, noe som har en avslappende effekt på glatte muskler. I tillegg anses prostaglandiner E2 som dominerende i begynnelsen av fødselen.
Medisiner
Preparater av prostaglandin E2-gruppen brukes. De vanligste, testede i praktisk obstetrikk, medisinske midlene for å forberede livmorhalsen på fødsel og fremkalle fødsel inkluderer preparater av prostaglandiner E2. Prostaglandiner E2 er tilgjengelige i forskjellige doseringsformer: i form av geler for intracervikal bruk, vaginale tabletter og pessarer. Effektiviteten til prostaglandiner E2 i å modne livmorhalsen og starte fødsel når 80–83 %. Imidlertid kan bruken av dem føre til utvikling av ukoordinert, voldsom fødsel og for tidlig løsning av en normalt plassert morkake. Følgelig bør prostaglandiner E2 kun administreres på fødesykehus med obligatorisk kardiotokografisk overvåking av fosterets hjerteaktivitet og livmorkontraktilitet.
Pasientopplæring
Nødvendigvis:
- lære kvinner å føre en menstruasjonskalender for å sikre evnen til å beregne svangerskapsalder og forfallsdato nøyaktig; telle fosterbevegelser for raskt å bestemme risikoen for fosterhypoksi når motorisk aktivitet avtar eller øker;
- informere pasienten om behovet for en grundig vurdering av fosterets tilstand ved en svangerskapsperiode på mer enn 40 uker og 3 dager og mulig sykehusinnleggelse i nærvær av ugunstige prognostiske faktorer.
Videre forvaltning
Standard for undersøkelse og behandling av kvinner med en svangerskapsperiode på over 40 uker:
- Utføre differensialdiagnostikk av posttermin og langvarig graviditet.
Posttermin graviditet bør vurderes i følgende tilfeller: første fødsel hos en gravid kvinne over 30 år, regelmessig menstruasjonssyklus, tidligere kjønnssykdommer og kroniske betennelsessykdommer i livmorvedhengene, indikasjon på sen fødsel, samsvar med svangerskapsalderen beregnet basert på første dag av siste menstruasjon og ultralyddata utført mellom 7. og 20. svangerskapsuke, ved «umoden» eller «utilstrekkelig moden» livmorhals, påvisning av morkake i stadium GIII eller oligohydramnion under ultralyd.
Langvarig graviditet indikeres av: den gravide kvinnens alder fra 20 til 30 år; dysfunksjon i eggstokkene med uregelmessig eller langvarig (> 35 dager) menstruasjonssyklus; avvik mellom svangerskapsalderen bestemt av den første dagen av siste menstruasjon og ultralyd; påvisning av en "moden" livmorhals; morkake med GI- og GIII-modenhet uten forsteininger og en normal mengde fostervann under ultralyd.
- For å kunne vurdere fosterets tilstand korrekt og forhindre uønskede perinatale utfall, må alle gravide kvinner med en svangerskapsperiode på mer enn 40 uker gjennomgå Doppler-ultralydundersøkelse av fosterets arterielle hemodynamikk.
- Hvis fosterets hemodynamikk er uendret, forberedes kroppen på fødsel ved bruk av østrogener, intracervikal administrering av prostaglandin E2-gel med dynamisk CTG-kontroll (daglig) og overvåking av fosterets blodstrøm (hver 3. dag).
- Når sentralisering av blodsirkulasjonen oppdages, er en studie av venøs blodstrøm og intrakardial hemodynamikk indikert for å avklare fosterets kompensasjonsevner og velge metode og tidspunkt for fødsel.
- Under graviditet etter termin endres fosterets hemodynamikk i stadier:
Fase I - forstyrrelser i intraplacental og føtalplacental blodstrøm. På dette stadiet er det ingen forstyrrelser i arteriell og venøs føtal hemodynamikk. En økning i vaskulær motstand observeres i navlestrengsarterien og dens terminale grener, så vel som i spiralarteriene. Indikatorene for gasssammensetning og syre-base-tilstand i navlestrengsblodet er innenfor normale grenser.
Stadium II - sentralisering av fosterets sirkulasjon. Hypoksemi observeres i den nyfødtes blod ved fødselen. På dette stadiet bør man skille mellom to påfølgende stadier:
- IIa - første tegn på sentralisering av føtal arteriell sirkulasjon med uendret venøs og intrakardial blodstrøm;
- IIb - moderat uttalt sentralisering av blodsirkulasjonen med nedsatt blodstrøm i venekanalen og økt blodstrømningshastighet i aortaklaffen.
Stadium III - uttalt sentralisering av fosterets sirkulasjon med nedsatt venøs utstrømning og dekompensasjon av sentral og intrakardial hemodynamikk. I navlestrengsblodet til den nyfødte ved fødselen - hypoksemi kombinert med acidose og hyperkapni.
- Hvis det oppdages redusert CPC (< 1,1), sentralisering av føtal hemodynamikk (initial sentralisering: SDO i MCA < 2,80; i Ao > 8,00) med en økning i gjennomsnittlig blodstrømningshastighet i venekanalen (moderat sentralisering: SDO i MCA < 2,80; i Ao > 8,00; Tamx i VP > 32 cm/s), og første tegn på føtal hypoksi i henhold til CTG-data, er intravenøs administrering av hesobendin + etamivan + etofillin indisert som prenatal forberedelse for å øke den adaptive kapasiteten til føtal hjerne.
- Ved initial sentralisering (SDO i MCA < 2,80; eller i fosterets aorta > 8,00) med god biologisk beredskap for fødsel, ukomplisert obstetrisk og gynekologisk sykehistorie, gjennomsnittlig fosterstørrelse, programmert fødsel gjennom den naturlige fødselskanalen etter amniotomi under nøye hjerteovervåking av fosterets kardiovaskulære system er mulig. Mangel på biologisk beredskap for fødsel, forverret obstetrisk og gynekologisk sykehistorie, stor fosterstørrelse dikterer behovet for planlagt keisersnitt.
- Ved moderat uttrykt sentralisering av føtal hemodynamikk (SDO i MCA < 2,80 og i aorta > 8,00; Tamx i VP > 32 cm/s) på grunn av spenningen i alle fosterets kompensasjonsmekanismer og mangel på reservekapasitet for fødsel, er keisersnitt indisert planlagt.
- Påvisning av forstyrrelser i både arterielle og venøse kanaler i føtal blodstrøm (markert sentralisering: SDO i MCA < 2,80 og i aorta > 8,00; i VPr S/A > 2,25, PIV > 1,00; i IVC %R > 16 %, PIV > 1,2) i kombinasjon med moderat eller alvorlig føtal hypoksi i henhold til CTG-data indikerer dekompensasjon av føtal hemodynamikk og krever fødsel med akutt keisersnitt.
Forebygging
- Identifisering av en risikogruppe for graviditet etter termin blant kvinner som søker svangerskapsomsorg.
- Forebygging av placentasvikt og for stort foster.
- Nøye beregning av svangerskapsperioden og fødselsdatoen, med tanke på datoen for siste menstruasjon (med regelmessig menstruasjonssyklus) og en ultralydsskanning utført før 20 ukers svangerskap.
- Rettidig sykehusinnleggelse av en gravid kvinne for å forberede fødselskanalen for fødsel og vurdere fosterets tilstand.
Prognose
Med rettidig og grundig vurdering av fosterets tilstand og tilstrekkelig obstetrisk taktikk er prognosen gunstig. Indikatorene for fysisk og nevropsykisk utvikling hos barn skiller seg ikke fra de ved ukompliserte, rettidige fødsler. Med utvikling av komplikasjoner, spesielt alvorlig fosterhypoksi, fødselstraumer og mekoniumaspirasjon, er prognosen imidlertid mindre gunstig. Perinatale tap er opptil 7 %, hypoksisk-iskemisk skade på sentralnervesystemet - opptil 72,1 %.


 [
[