
Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
Ny tilnærming blokkerer kreftcelletilpasning og dobler effektiviteten av cellegiftbehandling
Sist anmeldt: 27.07.2025
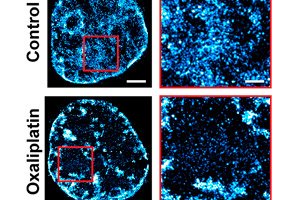
I en helt ny tilnærming til kreftbehandling har biomedisinske ingeniører fra Northwestern University doblet effektiviteten av cellegift i et dyreforsøk.
I stedet for å angripe kreften direkte, hindrer denne unike strategien kreftceller i å utvikle seg til å bli resistente mot behandlinger – noe som gjør sykdommen mer mottakelig for eksisterende legemidler. Ikke bare utryddet denne tilnærmingen sykdommen praktisk talt i cellekulturer, den forbedret også effektiviteten av cellegift betydelig i musemodeller av eggstokkreft.
Studien ble publisert i tidsskriftet Proceedings of the National Academy of Sciences.
«Kreftceller er gode tilpasningsevner», sier Vadim Backman fra Northwestern University, som ledet studien. «De kan tilpasse seg nesten hva som helst. Først lærer de hvordan de skal unngå immunforsvaret. Deretter lærer de hvordan de skal motstå cellegift, immunterapi og stråling. Når de blir resistente mot disse behandlingene, lever de lenger og får nye mutasjoner. Vi ønsket ikke å drepe kreftcellene direkte. Vi ønsket å ta bort superkraften deres – deres medfødte evne til å tilpasse seg, forandre seg og unngå.»
Backman er Sachs-familiens professor i biomedisinsk ingeniørfag og medisin ved Northwestern Universitys McCormick School of Engineering, hvor han leder Center for Physical Genomics and Engineering. Han er også medlem av Robert H. Leury Comprehensive Cancer Center, Institute for the Chemistry of Life Processes og International Nanoscience Institute.
Kromatin er nøkkelen til kreftoverlevelse
Kreft har mange særegne trekk, men én egenskap ligger til grunn for dem alle: dens ubarmhjertige evne til å overleve. Selv når immunforsvaret og aggressive medisinske behandlinger angriper en svulst, kan kreften krympe eller avta i vekst, men den forsvinner sjelden helt. Selv om genetiske mutasjoner bidrar til resistens, skjer mutasjonene for sakte til å forklare kreftcellenes raske respons på stress.
I en rekke studier avdekket Backmans team en grunnleggende mekanisme som forklarer denne evnen. Den komplekse organiseringen av genetisk materiale kalt kromatin bestemmer kreftens evne til å tilpasse seg og overleve selv de kraftigste medisinene.
Kromatin, en gruppe makromolekyler som inkluderer DNA, RNA og proteiner, bestemmer hvilke gener som undertrykkes og hvilke som uttrykkes. For å pakke de to meterne med DNA som utgjør genomet inn i et rom bare en hundredels millimeter inne i cellekjernen, er kromatin ekstremt kompakt.
Ved å kombinere avbildning, modellering, systemanalyse og in vivo-eksperimenter, fant Backmans team ut at 3D-arkitekturen til denne pakken ikke bare kontrollerer hvilke gener som aktiveres og hvordan celler reagerer på stress, men også lar celler fysisk kode et "minne" av gentranskripsjonsmønstre inn i selve pakkens geometri.
Den tredimensjonale strukturen i genomet fungerer som et selvlærende system, i likhet med en maskinlæringsalgoritme. Etter hvert som det «lærer», blir denne strukturen stadig omorganisert til tusenvis av nanoskopiske kromatinpakkedomener. Hvert domene lagrer en del av cellens transkripsjonsminne, som bestemmer hvordan cellen fungerer.
Omprogrammering av kromatin for å forbedre cellegiftbehandling
I den nye studien utviklet Backman og kollegene hans en beregningsmodell som bruker fysiske prinsipper for å analysere hvordan kromatinpakking påvirker en kreftcelles sannsynlighet for å overleve cellegiftbehandling. Ved å anvende modellen på ulike typer kreftceller og klasser av cellegiftmedisiner, fant teamet ut at det nøyaktig kunne forutsi celleoverlevelse – selv før behandlingen startet.
Fordi kromatinpakking er avgjørende for kreftcelleoverlevelse, spurte forskerne seg selv: hva ville skje hvis pakkearkitekturen ble endret? I stedet for å lage nye legemidler, undersøkte de hundrevis av eksisterende legemidler for å finne kandidater som kunne endre det fysiske miljøet inne i cellekjerner og påvirke kromatinpakking.
Til slutt valgte teamet celecoxib, et FDA-godkjent antiinflammatorisk legemiddel som allerede brukes til å behandle leddgikt og hjerte- og karsykdommer, og som som en bivirkning endrer pakningen av kromatin.
Eksperimentelle resultater
Ved å kombinere celecoxib med standard cellegiftbehandling, så forskerne en betydelig økning i antall kreftceller som døde.
I musemodeller av eggstokkreft reduserte en kombinasjon av paklitaksel (et vanlig cellegiftmiddel) og celecoxib tilpasningshastigheten til kreftcellene og forbedret undertrykkelsen av tumorvekst, noe som overgikk effekten av paklitaksel alene.
«Da vi brukte en lav dose cellegift, fortsatte svulstene å vokse. Men da vi la til en kandidat-TPR (transkripsjonell plastisitetsregulator) til cellegiften, så vi mye mer betydelig veksthemming. Det doblet effekten», sa Backman.
Mulige utsikter
Denne strategien kan gjøre det mulig for leger å bruke lavere doser cellegift, noe som reduserer alvorlige bivirkninger. Dette vil forbedre pasientenes komfort og deres opplevelse av kreftbehandlingen betydelig.
Backman mener at omprogrammering av kromatin kan være nøkkelen til å behandle andre komplekse sykdommer, inkludert hjerte- og karsykdommer og nevrodegenerative sykdommer.
