
Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
Hypofysemikroadenom: årsaker, symptomer, fare, prognose
Medisinsk ekspert av artikkelen
Sist anmeldt: 12.07.2025
Godartede neoplasmer som oppstår i de endokrine kjertlene kalles adenomer, og et mikroadenom i hypofysen er en liten svulst i den fremre loben, som produserer en rekke viktige hormoner.
Epidemiologi
Forekomsten av hypofysetumorer er anslått til å være 10–23 %, og hypofyseadenomer, som kan ha forskjellige former og størrelser, er de vanligste (16 %).[ 1 ]
Opptil 20–25 % av mennesker kan ha små hypofysesvulster, mikroadenomer, uten å vite om det, og slike svulster oppdages ved en tilfeldighet under hjerneavbildning i omtrent halvparten av tilfellene.
Prolaktinsekreterende mikroadenomer står for 45–75 % av slike svulster; ACTH-produserende formasjoner står for ikke mer enn 14 % av tilfellene, og hyppigheten av STH-produserende mikroadenomer overstiger ikke 2 %.
Mikroadenom i hypofysen hos barn og ungdom oppdages i 10,7–28 % av tilfellene, og minst halvparten av dem er hormonelt inaktive. [ 2 ]
Fører til hypofysære mikroadenomer
Eksperter vet ikke de eksakte årsakene til forekomsten av mikroadenom i hypofysen, en endokrin kjertel i hjernen hvis celler produserer:
- kortikotropin eller ACTH – adrenokortikotropisk hormon, som forårsaker utskillelse av steroidhormoner fra binyrebarken;
- veksthormon STH – somatotropisk hormon;
- gonadotropiner FSH – follikkelstimulerende hormon og LH – luteiniserende hormon, som bestemmer produksjonen av kvinnelige kjønnshormoner i eggstokkene og mannlige kjønnshormoner i testiklene;
- laktogent hormon prolaktin (PRL);
- tyreotropin eller tyreoidstimulerende hormon (TSH), som stimulerer syntesen av hormoner i skjoldbruskkjertelen.
Det antas at utviklingen av disse neoplasmene kan være forårsaket av traumatisk hjerneskade; utilstrekkelig blodtilførsel til hypofysen; hjerneinfeksjoner eller eksponering for giftstoffer (som forårsaker ødem og intrakraniell hypertensjon).
Risikofaktorer
Det er kjent at hypofyseadenomer og mikroadenomer forekommer oftere ved familiehistorie med MEN 1-syndrom – multippel endokrin adenomatose type 1, som er arvelig. Det finnes dermed genetisk bestemte risikofaktorer knyttet til visse endringer i DNA. [ 3 ]
Multippel endokrin neoplasi type 4 (MEN4): MEN 4 har en mutasjon i genet for cyklinavhengig kinasehemmer 1 B (CDKN1B), som er karakterisert av hypofysetumorer, hyperparatyreoidisme, nevroendokrine svulster i testiklene og livmorhalsen.[ 4 ]
Carney-kompleks (CNC): Ved Carney-komplekset er det en kimlinjemutasjon i tumorsuppressorgenet PRKAR1A som fører til primær pigmentert nodulær adrenokortikal sykdom (PPNAD), testikulære svulster, skjoldbruskkjertelknuter, flekkvis hyperpigmentering av huden og akromegali.[ 5 ]
Den kliniske formen for familiære isolerte hypofyseadenomer (FIPA) er karakterisert av genetiske defekter i arylhydrokarbonreseptor-interagerende protein (AIP)-genet, i omtrent 15 % av alle relaterte og 50 % av homogene somatotropinfamilier.[ 6 ]
Familiære isolerte hypofyseadenomer (FIPA): En mutasjon i arylhydrokarbonreseptor-interaksjonsproteinet (AIP) oppdages i ungdomsårene eller tidlig voksen alder i omtrent 15 % av alle FIPA-tilfeller. Disse svulstene er vanligvis aggressive og skiller oftest ut veksthormon, noe som forårsaker akromegali.[ 7 ]
Muligheten for at denne typen svulst oppstår som følge av funksjonsforstyrrelser hos andre endokrine kjertler og hjernestrukturer, spesielt endringer i hypothalamus vaskulære system, som innenfor det nevroendokrine hypothalamus-hypofysesystemet regulerer funksjonen til hypofysen og dens fremre lob, adenohypofysen, med dens frigjørende hormoner, er ikke utelukket.
Patogenesen
I følge histologien er hypofyseadenom en godartet svulst; avhengig av størrelsen er disse neoplasmene delt inn i mikroadenomer (opptil 10 mm i størrelse på det bredeste punktet), makroadenomer (10-40 mm) og gigantiske adenomer (40 mm eller mer).
Mens man studerer patogenesen til tumordannelse i hypofysen, har det ennå ikke vært mulig å bestemme mekanismene for hyperplastisk transformasjon av celler i dens fremre lob til en tumor.
Eksperter mener at en av de mest overbevisende versjonene er en sammenheng med dereguleringen av metabolismen til nevrotransmitteren og hormonet dopamin (som er den viktigste hemmeren av prolaktinsekresjon) og/eller en forstyrrelse av funksjonene til transmembrane dopaminreseptorer i hypofyseceller som utskiller PRL (laktotrofer).
De fleste hypofysemikroadenomer er sporadiske, men noen forekommer som en del av genetisk bestemte nevroendokrine syndromer som MEN 1, McCune-Albright syndrom, Werners syndrom og Carney syndrom (eller Carney-komplekset). Sistnevnte er assosiert med økt risiko for å utvikle godartede svulster i hormonelle (endokrine) kjertler, inkludert hypofysen, binyrene, skjoldbruskkjertelen, eggstokkene og testiklene.
Symptomer hypofysære mikroadenomer
Et hypofyse-mikroadenom kan være symptomerløst over lang tid. Symptomene varierer avhengig av plassering og oppstår vanligvis som et resultat av endokrin dysfunksjon. Dette er det vanligste funnet i tilfeller av hormonell ubalanse forbundet med overdreven produksjon av ett eller flere hormoner. I de fleste tilfeller, basert på plassering, er dette et mikroadenom i den fremre hypofysen.
Det finnes forskjellige typer hypofysemikroadenom basert på deres hormonelle aktivitet. Den vanligste typen anses derfor å være et ikke-fungerende adenom – et hormonelt inaktivt hypofysemikroadenom, som – inntil det når en viss størrelse – ikke gir noen symptomer. Men et voksende hormonelt inaktivt hypofysemikroadenom kan komprimere nærliggende hjernestrukturer eller hjernenerver, slik at et hypofysemikroadenom og hodepine i frontal- og temporalregionene kan kombineres, [ 8 ] og synsproblemer er også mulig. [ 9 ] Imidlertid, som forskere hevder, er ikke-fungerende (hormonelt inaktive) hypofysesvulster i 96,5 % av tilfellene makroadenomer. [ 10 ]
Hormonelt aktivt mikroadenom i hypofysen (den fremre lobben) med økt utskillelse av hormonet prolaktin kan også forekomme - prolaktinom i hypofysen. Økt produksjon av PRL av laktotrope celler i adenohypofysen er definert som hyperprolaktinemi ved hypofysemikroadenom.
Hvordan manifesterer et slikt hypofyse-mikroadenom seg hos kvinner? Patologisk høye nivåer av dette hormonet hemmer produksjonen av østrogener, og de første tegnene manifesteres av menstruasjonssyklusforstyrrelser - med fravær av menstruasjon (amenoré) og/eller eggløsningsfasen. Som et resultat utvikles vedvarende galaktoré-amenoré-syndrom, og evnen til å bli gravid og bli gravid går tapt.
Prolaktinsekreterende hypofysemikroadenom hos menn kan føre til hyperprolaktinemisk hypogonadisme med redusert libido, erektil dysfunksjon, forstørrede bryster (gynekomasti) og redusert ansikts- og kroppshår.
Aktivt mikroadem som utskiller kortikotropin (ACTH) fører til et overskudd av steroidhormoner (glukokortikoider) produsert av binyrebarken, noe som kan forårsake Itsenko-Cushings sykdom i hypofysen.
Hos barn kan et slikt mikroadenom manifestere seg med symptomer på hyperkortisisme (Cushings syndrom), inkludert hodepine, generell svakhet, overflødig avsetning av fettvev på kroppen, redusert bentetthet og muskelstyrke, stripelignende atrofi av huden (i form av lilla strier), etc.
Med et aktivt somatotropinproduserende mikroadenom øker nivået av STH i kroppen. I barndommen stimulerer den overdrevne anabole effekten veksten av nesten alle bein i kroppen og kan føre til gigantisme; hos voksne kan akromegali utvikle seg med økt vekst av ansiktsbein (forårsaker forvrengning av utseende) og brusk i leddene i ekstremitetene (som fører til et brudd på deres proporsjoner og fortykkelse av fingrene), med leddsmerter, overdreven svetting og talgproduksjon, og nedsatt glukosetoleranse.
Svært sjelden (i 1-1,5 % av tilfellene) er det et mikroadenom i hypofysen som produserer tyreotropin, og siden dette hormonet har en stimulerende effekt på skjoldbruskkjertelen, har pasienter kliniske tegn på hypofysehypertyreose i form av sinus takykardi og atrieflimmer i hjertet, økt blodtrykk, redusert kroppsvekt (med økt appetitt), samt økt nervøs eksitabilitet og irritabilitet.
Det såkalte intrasellære mikroadenomet i hypofysen, synonymt - endosellært mikroadenom i hypofysen, er, i likhet med hele hypofysen, lokalisert i sella turcica - inne i den anatomiske salformede fordypningen i kilebenet ved hodeskallens base. Samtidig ligger hypofysen nederst i denne fordypningen - i hypofysefossa (intrasellær region). Og hele forskjellen i ordvalg er at "inne" på latin er intra, og på gresk - endom.
Men et hypofysemikroadenom med suprasellær vekst betyr at neoplasmen vokser oppover fra bunnen av hypofysefossa.
Cystisk mikroadenom i hypofysen har en lukket sekklignende struktur og er en asymptomatisk formasjon.
Mikroadenom i hypofysen med blødning kan være et resultat av apopleksi eller hemoragisk infarkt assosiert med forstørrelse av kjertelen og skade på sinusformede kapillærer i parenkymet i dens fremre lob, nevrohemale synapser og/eller portalkar.
Mikroadenom i hypofysen og graviditet
Som allerede nevnt er kvinner med prolaktinproduserende hypofysemikroadenom vanligvis infertile på grunn av østrogenmangel og undertrykkelse av pulserende sekresjon av GnRH (gonadotropinfrigjørende hormon). For å bli gravid må prolaktinnivåene normaliseres, ellers skjer ikke unnfangelse, eller svangerskapet avbrytes helt i begynnelsen.
- Er det mulig å føde med et hypofyse-mikroadenom?
Hos kvinner med klinisk fungerende mikroadenomer som behandles med dopaminagonister (kabergolin eller dostinex), kan prolaktinnivåene normaliseres og menstruasjonssykluser og fertilitet kan gjenopprettes.
Er amming mulig med hypofyse-mikroadenom?
I barselperioden er amming tillatt hvis det ikke er noen symptomer på svulsten, men det er nødvendig å overvåke størrelsen (ved hjelp av magnetisk resonansavbildning av hjernen). Og hvis svulsten vokser, stoppes ammingen.
- Mikroadenom i hypofysen og IVF
Behandling av hyperprolaktinemi er nødvendig for IVF, og prosedyren kan igangsettes dersom normale prolaktinnivåer har vært stabile i 12 måneder og det ikke er noen unormaliteter i serumnivåene av andre hypofysehormoner.
Komplikasjoner og konsekvenser
Hva er farlig med hypofysemikroadenom? Selv om denne svulsten er godartet, kan dens tilstedeværelse forårsake komplikasjoner og ha konsekvenser, spesielt:
- føre til dysfunksjon av hypothalamus-hypofysen-binyresystemet med utviklingen av Itsenko-Cushings sykdom;
- forstyrre hormonreguleringen av menstruasjonssyklusen hos kvinner og føre til erektil dysfunksjon hos menn;
- forårsake veksthemming og hypofysedvergvekst (hypopituitarisme) hos barn;
- provosere utviklingen av osteoporose.
Når en voksende svulst komprimerer synsnervefibrene i kryssingsområdet deres (som hos 80 % av mennesker ligger rett over hypofysen), oppstår det en forstyrrelse i øyets mobilitet (oftalmoplegi) og en gradvis forverring av det perifere synet. Selv om mikroadenomer vanligvis er for små til å utøve et slikt trykk.
Kan et hypofyse-mikroadenom forsvinne? Det kan ikke forsvinne, men over tid kan en hormonelt inaktiv svulst hos barn reduseres betydelig. Men hos omtrent 10 % av pasientene kan mikroadenomer øke i størrelse.
Diagnostikk hypofysære mikroadenomer
For å diagnostisere et hypofysemikroadenom kreves en fullstendig sykehistorie og laboratorietester: blodprøver for hormonnivåer (produsert av hypofysen), inkludert en radioimmunoassay av blodserum for prolaktinnivåer.
Hvis prolaktin er normalt med et hypofyse-mikroadenom, er denne svulsten hormonelt inaktiv. Men hvis det er symptomer på prolaktinom, kan et slikt falskt negativt resultat enten være et resultat av en laboratorietestfeil, eller at pasienten har utviklet et makroadenom som komprimerer hypofysestilken.
I tillegg kan det være nødvendig med ytterligere tester, for eksempel for nivået av skjoldbruskkjertelhormoner (T3 og T4), immunglobuliner, interleukin-6 i blodserumet.
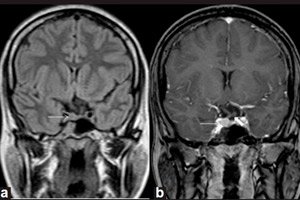
Mikroadenom kan kun oppdages ved instrumentell diagnostikk ved bruk av magnetisk resonansavbildning (MR) av hjernen. Og MR for mikroadenom regnes som standarden for visualisering, med en sensitivitet på 90 % for MR med kontrastforsterkning.
MR-tegn på hypofysemikroadenom inkluderer: volum av kjertelen på siden av mikroadenomet; en økning i størrelsen på sella turcica; tynning og endringer i konturen av fundus (nedre vegg); lateral avvikelse av hypofysens infundibulum; isointensitet av det avrundede området sammenlignet med grå substans på T1- og T2-vektede bilder; lett hyperintensitet på T2-vektede bilder. [ 11 ]
Differensiell diagnose
Differensialdiagnostikk utføres med kraniofaryngeom, granulær celletumor (koristom) i hypofysen, Rathkes pouchcyste, dermoiddannelse, betennelse i hypofysen - autoimmun eller lymfocytisk hypofysitt, feokromocytom, skjoldbruskkjertelsykdommer, etc.
Hos kvinner med anovulatorisk syklus er det differensiert mellom hypofysemikroadenom og polycystisk ovariesyndrom, siden 75–90 % av tilfellene med manglende eggløsning er en konsekvens av polycystisk ovariesyndrom.
Hvem skal kontakte?
Behandling hypofysære mikroadenomer
Ved adenomer og mikroadenomer i hypofysen kan behandlingen være medisinsk og kirurgisk. Samtidig, hvis svulstene er asymptomatiske, anbefales det å overvåke dem, det vil si å utføre MR med jevne mellomrom, for ikke å gå glipp av begynnelsen på forstørrelsen.
Resepten på et bestemt legemiddel bestemmes av hvilken type svulst pasienten har.
Farmakoterapi av svulster som utskiller PRL utføres med legemidler fra gruppen stimulatorer av dopamin D2-reseptorer i hypothalamus (selektive dopaminagonister), og de mest brukte er bromokriptin (Parlodel, Bromergol), Norprolac og ergotderivatet Cabergoline eller Dostinex for hypofysemikroadenom med økt prolaktinsekresjon.
Bivirkninger av Dostinex (kabergolin) kan omfatte allergiske reaksjoner; hodepine og svimmelhet; kvalme, oppkast og magesmerter; forstoppelse; følelse av svakhet eller tretthet; søvnforstyrrelser. Blant bivirkningene av bromokriptin (i tillegg til allergiske reaksjoner) er brystsmerter; økt hjertefrekvens og pust med følelse av kortpustethet; hoste opp blod; forverring av koordinasjonen av bevegelser, osv.
Legemidlene oktreotid (sandostatin), lanreotid (somatulin) og pegvisomant, som brukes mot mikro- og makroadenomer som skiller ut veksthormon, er hemmere av STH og antagonister av dets reseptorer.
Og for ACTH-sekrerende neoplasmer i adenohypofysen med Itsenko-Cushing syndrom, brukes metyrapon (Metopiron) eller mitotan (Lysodren).
Kirurgisk behandling bør vurderes for fungerende (hormonelt aktive) mikroadenomer. I tilfeller der konservativ behandling er ineffektiv og svulsten har en liten suprasellær ekspansjon i sella turcica, kan hypofyseadenomektomi foreskrives – en operasjon for å fjerne hypofysemikroadenomet. For tiden utføres transnasal eller transsfenoidal mikrodisseksjon, det vil si fjerning av hypofysemikroadenomet gjennom nesen.
Mulige komplikasjoner og konsekvenser av fjerning av hypofysemikroadenom inkluderer postoperativ blødning og lekkasje av cerebrospinalvæske (som ofte krever reoperasjon), samt betennelse i hjernehinnene, synshemming, hematomdannelse, forbigående diabetes insipidus og tilbakefall av mikroadenomet.
Homeopati for hypofysemikroadenom med hyperprolaktinemi bruker legemidler hvis virkning kan bidra til å delvis lindre symptomer. For eksempel, for uregelmessig menstruasjon og amenoré, foreskrives et middel laget av blekksprutblekk Sepia og et middel laget av engpasqueblomstplanten Pulsatilla, og for galaktoré foreskrives et middel basert på roten av europeisk cyclamen.
Det er åpenbart at man ikke bør håpe at folkebehandling for hypofyse-mikroadenom kan være mer effektiv. Og ikke bare fordi urtemedisinere med denne diagnosen kun lar seg veilede av pasientenes klager (uten å kjenne deres sanne etiologi), men også på grunn av upåliteligheten til mange "folkemedisiner". Du trenger ikke å gå langt for eksempler.
Noen internettkilder anbefaler å bruke en blanding av primula, ingefærrot og sesamfrø for å redusere prolaktinnivåene. Men primula hjelper mot langvarig tørrhoste og tynnende slim, og ingefærrot, i likhet med sesamfrø, viser laktogene egenskaper.
Du kan også finne råd om å ta en tinktur av gresshoppa. Men i virkeligheten brukes dette middelet innvortes mot luft i magen og utvortes mot revmatiske leddsmerter. Etter all sannsynlighet ble løvhoppa forvekslet med røttene til klaseormedrue (andre navn på den er klaseormedrue og svart klaseormedrue), som brukes mot hetetokter i overgangsalderen.
Ernæring for hypofysemikroadenom bør være balansert - med redusert sukker- og saltinntak. Dette er ikke en spesiell diett, men rett og slett mindre kalorier.
Alkohol er utelukket ved hypofysemikroadenom.
Hvilken lege bør jeg oppsøke for et hypofyse-mikroadenom? Endokrinologer, gynekologer og nevrokirurger håndterer problemene som oppstår med denne typen svulst.
Forebygging
Fordi miljømessige eller livsstilsmessige årsaker til hypofysetumorer er ukjente, finnes det rett og slett ingen måte å forhindre utviklingen av hypofysemikroadenomer.
Prognose
De fleste hypofysetumorer er kurerbare. Hvis et hormonelt aktivt hypofysemikroadenom diagnostiseres i tide, er sjansene for bedring høye og prognosen gunstig.
Funksjonshemming og hypofysemikroadenom: Funksjonshemming kan være forbundet med tumorvekst og skade på synsnerven, samt andre konsekvenser av denne patologien, hvis alvorlighetsgrad er individuell. Og anerkjennelse av en pasient som funksjonshemmet avhenger av eksisterende helseproblemer og nivået av funksjonsforstyrrelser, som må oppfylle lovpålagte kriterier.
Mikroadenom i hypofysen og hæren: pasienter med denne svulsten (selv om den er fjernet) bør ikke overopphetes, oppholde seg i solen over lengre tid og overanstrenge seg fysisk. De er derfor ikke egnet for militærtjeneste.
Hvor lenge lever folk med hypofyse-mikroadenom? Denne svulsten er ikke kreft, så det er ingen grenser for forventet levealder. Selv om pasienter med aktivt STH-produserende mikroadenom kan utvikle hypertensjon og en økning i hjertestørrelse, og dette kan redusere forventet levealder betydelig. En økt risiko for død hos pasienter over 45 år er observert med Itsenko-Cushings sykdom og akromegali.

