
Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
Hepatitt A-virus
Medisinsk ekspert av artikkelen
Sist anmeldt: 04.07.2025
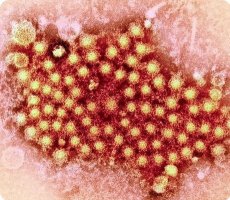
Viral hepatitt A er en smittsom sykdom hos mennesker, primært karakterisert av leverskade og klinisk manifestert ved rus og gulsott. Hepatitt A-viruset ble oppdaget i 1973 av S. Feinstone (et al.) ved hjelp av immunelektronmikroskopi og ved å infisere aper - sjimpanser og silkeaper. Essensen av immunelektronmikroskopimetoden er at spesifikke antistoffer (rekonvalesent serum) tilsettes filtratet av avføringen til en pasient med hepatitt A, og sedimentet utsettes for elektronmikroskopi. På grunn av virusenes interaksjon med spesifikke antistoffer, gjennomgår de spesifikk aggregering. I dette tilfellet er de lettere å oppdage, og aggregering under påvirkning av antistoffer bekrefter patogenets spesifisitet. S. Feinstones oppdagelse ble bekreftet i eksperimenter på frivillige.
Hepatitt A-viruset er sfærisk, viriondiameteren er 27 nm. Genomet er representert av enkelttrådet positivt RNA med mm 2,6 MD. Det finnes ingen superkapsid. Symmetritypen er kubisk - ikosaeder. Kapsiden har 32 kapsomerer, den er dannet av fire polypeptider (VP1-VP4). I henhold til egenskapene tilhører hepatitt A-viruset slekten Heparnovirus, familien Picornaviridae. Når det gjelder antigener, er hepatitt A-viruset (HAV - hepatitt A-virus) homogent. HAV reproduserer seg godt i kroppen til sjimpanser, bavianer, hamadryasbavianer og marmosetaper. I lang tid kunne ikke viruset dyrkes. Først på 1980-tallet var det mulig å få tak i cellekulturer der HAV reproduserer seg. I utgangspunktet ble kontinuerlige cellelinjer av rhesusmakakembryonyre (kultur FRhK-4) brukt til disse formålene, og nå brukes en kontinuerlig cellelinje av grønne apenyreceller (kultur 4647).
I henhold til anbefalingene fra WHO-eksperter er følgende nomenklatur for hepatitt A-virusmarkører tatt i bruk: hepatitt A-virus - HAV-antistoffer mot hepatitt A-virus: anti-HAV IgM og anti-HAV IgG.
HAV er en liten partikkel med en diameter på 27–30 nm, med ikosaedrisk symmetri og homogenitet. Elektronogrammet oppnådd ved hjelp av immunaggregeringsmetoden avslører elektrontette partikler med overfladisk plasserte symmetrisk anordnede kapsomerer. Ved negativ kontrast avsløres både fulle og tomme partikler i preparatene. Nukleokapsidet til HAV, i motsetning til influensa, har ikke overflatefremspring og en membran. Det er også viktig at HAV-virionet ikke har en hjerteformet struktur.
Basert på dets fysikalsk-kjemiske egenskaper er hepatitt A-viruset klassifisert som tilhørende picornavirusfamilien, enterovirusslekten med serienummer 72. Denne taksonomien viste seg imidlertid å være for uvanlig, og WHO anså det som mulig å beholde terminologien «hepatitt A-virus».
Som alle virus i Picornaviridae-familien inneholder hepatitt A-viruset ribonukleinsyre. Noen laboratorier har vist muligheten for å klone hepatitt A-virusgenomet, noe som åpner opp for muligheten for å få tak i vaksiner.
Resistens mot hepatitt A-virus
Viruset er relativt motstandsdyktig mot høye temperaturer, syrer, fettløsemidler (ingen lipider), desinfeksjonsmidler og tolererer lave temperaturer godt. Alt dette bidrar til dets langsiktige bevaring i det ytre miljøet. Ved romtemperatur overlever det i flere uker, ved 60 °C mister det delvis sin smittsomhet etter 4–12 timer, og helt etter flere minutter ved 85 °C. Det er svært motstandsdyktig mot klor, noe som gjør det i stand til å trenge inn i springvann gjennom barrierene i vannbehandlingsanlegg.
Oppsummert kan vi karakterisere hepatitt A-viruset som følger:
- den naturlige verten er mennesket;
- forsøksdyr - silkeaber, sjimpanser;
- kilden til infeksjon er avføring;
- sykdommen er epidemisk og endemisk;
- smittevei: feko-oral;
- inkubasjonsperiode - 14-40 dager;
- overgang til kronisk hepatitt - ikke observert.
De immunologiske egenskapene til HAV er som følger:
- Prototypiske stammer - Ms-1, CR-326, GВG. Alle er immunologisk like eller identiske;
- Antistoffer - IgM og IgG, produseres som respons på introduksjon av strukturelle proteiner i viruset og er beskyttende;
- I. Den beskyttende effekten av humant serumgammaglobulin – forebygger eller demper sykdommen hvis det administreres før infeksjon eller i inkubasjonsperioden.
De fysikalsk-kjemiske egenskapene til NAU er som følger:
- Morfologi: skallløs sfærisk partikkel med kubisk symmetri, kapsid består av 32 kapsomerer;
- Diameter - 27–30 nm;
- Tetthet i CsCl (g/cm3) - 1,38–1,46 (åpne partikler), 1,33–1,34 (modent virion), 1,29–1,31 (umodne virioner, tomme partikler);
- Sedimentasjonskoeffisient - 156–160 modne virioner;
- Nukleinsyre er et enkelttrådet, lineært RNA;
- Relativ molekylvekt - 2,25 10⁶–2,8 10⁶KD;
- Antall nukleotider er 6 500–8 100.
Stabiliteten til HAV under fysiske og kjemiske påvirkninger er som følger:
- Kloroform, eter - stabil;
- Klor, 0,5–1,5 mg/l, 5 °C, 15 min – delvis inaktivering;
- Kloramin, 1 g/l, 20 °C, 15 min - fullstendig inaktivering;
- Formalin, 1:4000, 35–37 °C, 72 timer – fullstendig inaktivering, 1:350, 20 °C, 60 min – delvis inaktivering.
Temperatur:
- 20–70 °C – stabil;
- 56 °C, 30 min - stabil;
- 60 °C, 12 timer - delvis inaktivering;
- 85 °C, 1 min - fullstendig inaktivering;
- Autoklavering, 120 °C. 20 min - fullstendig inaktivering;
- Tørr varme, 180 °C, 1 time – fullstendig inaktivering;
- UFO, 1,1 W, 1 min – fullstendig inaktivering.
De presenterte dataene viser at hepatitt A-viruset er nærmest enterovirus når det gjelder sine fysisk-kjemiske egenskaper. I likhet med andre enterovirus er HAV resistent mot mange desinfiseringsløsninger og inaktiveres fullstendig i løpet av få minutter ved 85 °C og autoklavering.
Det er bevist at hepatitt A-viruset kan reprodusere seg i primære og kontinuerlige monolagslinjer av cellekulturer fra mennesker og aper. Spesielt aktiv reproduksjon av hepatitt A-viruset i in vitro-kulturer observeres når leverekstrakter fra syke aper brukes som utgangsmateriale. Det skal imidlertid bemerkes at i alle eksperimenter på reproduksjon av hepatitt A-viruset på in vitro-kulturer rettes oppmerksomheten mot den lange inkubasjonsperioden under primære passasjer (opptil 4–10 uker), deretter øker akkumuleringen av viralt genetisk materiale, men de absolutte verdiene forblir svært ubetydelige, noe som gir grunnlag for mange forskere til å snakke om ufullstendig replikasjon av hepatitt A-viruset i vevskulturer.
Når man oppsummerer litteraturdataene om reproduksjon av hepatitt A-virus i ekstravevskulturer, kan man si at det er uten tvil at HAV overlever på lang sikt in vitro. Optimale forhold for et stabilt høyt nivå av virusreplikasjon er ikke endelig identifisert, og dette hindrer studiet av dets biologiske egenskaper, og det å skaffe en kilde til reagenser for produksjon av diagnostikk og vaksinedesign.
Samtidig kan man i litteraturen finne mer optimistiske vurderinger av dette problemet. Løsningen på alle spørsmål knyttet til dyrking av hepatitt A-viruset er et spørsmål om nær fremtid. Når man studerte de optimale forholdene for reproduksjon av HAV i kulturen av embryonale nyreceller fra rhesusmakaken, ble det identifisert to faser: fasen med produksjon av det smittsomme viruset (opptil 6-8 dager på nivået av den 5. passasje) og fasen med intensiv akkumulering av virusantigenet. Det ble også vist at den mest betydelige akkumuleringen av virusantigenet skjer under forholdene med såkalt rulledyrking (roterende kolber). Denne metoden åpner for store muligheter for å oppnå kulturelt antigen i store mengder, og følgelig vil kildematerialet for fremstilling av diagnostiske systemer og produksjon av vaksiner dukke opp.
Epidemiologi av hepatitt A
Hepatitt A-viruset er svært patogent for mennesker. Ifølge WHO (1987) er infeksjon med bare ett virion nok til å forårsake sykdommen. Imidlertid er den praktiske smittedosen sannsynligvis mye høyere. Den eneste smittekilden er en smittet person. Viruset skilles ut i store mengder med avføring 12–14 dager før gulsott og i løpet av de tre ukene av den ikteriske perioden. Det er ikke funnet noen signifikante forskjeller i utskillelsen av patogenet hos pasienter med ikteriske, anikteriske og asymptomatiske former for hepatitt A. Smitteveien er fekal-oral, hovedsakelig vannbåren, samt husholdnings- og matbåren. Smitteveien er fekal-oral, hovedsakelig vannbåren, samt husholdnings- og matbåren. Den viktigste (primære) overføringsveien for viruset er vannbåren. Smitte via luftbårne dråper er også mulig. Befolkningens mottakelighet er universell. For det meste er barn under 14 år rammet. Sykdommen har en uttalt høst-vinter sesongmessighet.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Symptomer på hepatitt A
Inkubasjonsperioden varierer fra 15 til 50 dager, avhengig av virusets infeksjonsdose, men er i gjennomsnitt 28–30 dager. Når hepatitt A-viruset er i kroppen, multipliserer det seg i de regionale lymfeknutene, trenger inn i blodet og deretter i levercellene og forårsaker akutt diffus hepatitt, som er ledsaget av skade på hepatocytter og retikuloendoteliale elementer i leveren og en reduksjon i avgiftnings- og barrierefunksjonene. Skade på hepatocytter oppstår ikke på grunn av virusets direkte virkning, men som et resultat av immunopatologiske mekanismer. Det mest typiske bildet av hepatitt A er en akutt ikterisk syklisk form: inkubasjonsperiode, prodromal (pre-ikterisk), ikterisk periode og rekonvalesens. Imidlertid oppdages et stort antall pasienter med anikteriske og asymptomatiske infeksjonsformer i infeksjonsfokusene, hvorav antallet er betydelig mer enn ikteriske ("isfjellfenomen").
Immunitet etter infeksjon er sterk og langvarig, forårsaket av virusnøytraliserende antistoffer og immunhukommelsesceller.
Mikrobiologisk diagnostikk av hepatitt A
Diagnostikk av hepatitt A (med unntak av infeksjon hos dyr - sjimpanser, marmoseter, bavianer, som vi ikke har) er basert på ulike immunologiske metoder: RSC, immunofluorescensmetode, hemagglutinering av immunadhesjon (komplekset av viralt antigen + antistoff i nærvær av komplement adsorberes på erytrocytter og forårsaker deres liming). Mulighetene for å bruke disse metodene er imidlertid begrensede på grunn av mangel på spesifikke virale antigener, og immunofluorescensreaksjonen krever leverbiopsi, noe som er uønsket. Metoden med immunelektronmikroskopi er pålitelig og spesifikk, men den er svært arbeidskrevende. Derfor er den eneste akseptable immunologiske reaksjonen så langt metoden med immunosorbentanalyse av den faste fasen i form av IFM eller RIM, spesielt i modifiseringen av "fangst" av immunoglobuliner av klasse M. I vårt land er et testsystem blitt foreslått for dette formålet - "DIAGN-A-HEP". Prinsippet for virkemåten til dette testsystemet er som følger. Først sorberes antistoffer mot immunglobuliner av klasse M (antiimmunglobuliner M) på veggene i polystyrenbrønner, deretter tilsettes pasientens serum som skal testes. Hvis det inneholder IgM-antistoffer, vil de binde seg til antistoffer av klasse M, deretter tilsettes et spesifikt viralt antigen (hepatitt A-virus), som oppnås ved dyrking i cellekultur. Systemet vaskes, og antivirale antistoffer merket med pepperrotperoksidase tilsettes det. Hvis alle fire komponentene i systemet samhandler, dannes en firelags "sandwich":
- antiimmunoglobuliner M,
- immunoglobuliner M (mot hepatitt A-viruset - i pasientens serum som studeres),
- viralt antigen,
- enzymmerkede antivirale antistoffer.
For å detektere dette komplekset tilsettes et substrat for enzymet i brønnene. Under påvirkning av enzymet ødelegges det, og et farget produkt dannes. Fargeintensiteten kan måles kvantitativt ved hjelp av et spektrofotometer eller fotokolorimeter.
Fordelen med IgM-"fangstmetoden" er at antistoffer av denne klassen immunoglobuliner dukker opp under den primære immunresponsen og indikerer det aktive infeksjonsstadiet. De forsvinner etter at sykdommen er oppstått. Antivirale antistoffer som tilhører IgG-klassen, derimot, vedvarer lenge etter at sykdommen er oppstått, og gir ervervet immunitet. En DNA-probemetode er foreslått for å påvise hepatitt A-virus: komplementært vRNA-DNA brukes som probe.
Spesifikk forebygging av hepatitt A
Tidligere mye brukt seroprofylakse mot hepatitt A med gammaglobulin rettferdiggjorde seg ikke, derfor ble hovedvekten lagt på å gjennomføre vaksinasjonsprofylakse, og vaksinasjon mot hepatitt A utføres. For dette formålet utvikles og brukes ulike typer vaksiner allerede. I Russland ble en effektiv vaksine mot hepatitt A anskaffet tilbake i 1995, og den brukes nå med suksess.

